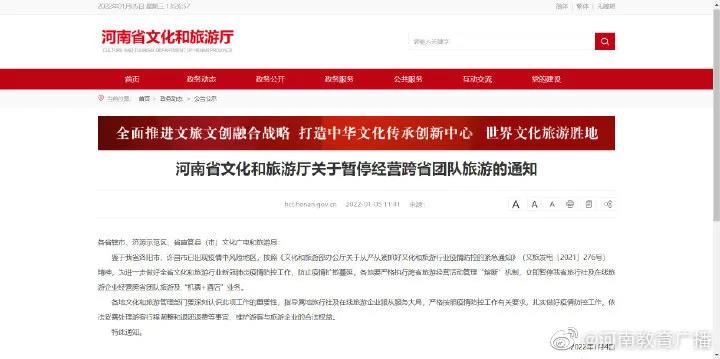
·阿爾茨海默病基因研究先驅(qū)魯?shù)婪颉ぬ过R曾說(shuō)到,罕見(jiàn)變異在人群中的發(fā)生頻率低于1%,卻占個(gè)體基因組變異的77%,僅使用全基因組關(guān)聯(lián)研究(GWAS)可能會(huì)錯(cuò)過(guò)疾病的大部分遺傳景觀。
時(shí)隔百年,與探究阿爾茨海默病理機(jī)制密切相關(guān)的兩位女性。
 (資料圖片)
(資料圖片)
逃離阿爾茨海默病的命運(yùn)
1906年,55歲的奧古斯特·德特女士(Auguste Deter)去世,德國(guó)精神病學(xué)家阿爾茨海默(Alois Alzheimer)解剖了她已經(jīng)萎縮的大腦,發(fā)現(xiàn)其中滲透有微小的斑塊,還有奇怪的纏結(jié)標(biāo)記神經(jīng)元的死亡,足以將她的疾病與其他的癡呆癥區(qū)分開(kāi)來(lái)。它們被后世命名為β淀粉樣蛋白(Aβ)和tau蛋白,成為阿爾茨海默病的獨(dú)特標(biāo)志物。
一百多年后,哥倫比亞安蒂奧基亞的艾麗婭(Aliria Rosa Piedrahita de Villegas)被研究人員稱作“我們時(shí)代的奧古斯特”。她所在的大家庭擁有一種罕見(jiàn)的遺傳性基因突變,幾乎可以確保她在40歲左右就會(huì)罹患早發(fā)性阿爾茨海默病。然而,直到72歲,她才出現(xiàn)輕微的癥狀。2020年11月,她因黑色素瘤去世,享年77歲,離開(kāi)前幾個(gè)月仍記得家人和朋友、自己做飯和洗澡,并且可以毫不費(fèi)力地記住“神經(jīng)科學(xué)”和“冠狀病毒”之類的名詞。
艾麗婭究竟如何逃過(guò)了被阿爾茨海默病“詛咒”的命運(yùn),長(zhǎng)久吸引著科學(xué)家的目光。此前他們已經(jīng)通過(guò)腦核成像技術(shù)發(fā)現(xiàn),她的大腦里含有大量Aβ,卻沒(méi)有多少tau蛋白,在普通患者中,兩者往往先后出現(xiàn)和累加。艾麗婭的獨(dú)特之處在于,她除了具有家族遺傳的致病基因突變PSEN1 E280A之外,她還有一個(gè)極其罕見(jiàn)的基因突變——APOE3 Christchurch,且是來(lái)自父母雙方的純合子(其他人只有來(lái)自父母一方的一個(gè)基因突變拷貝)。
在APOE的3個(gè)等位基因中,APOE4被公認(rèn)為阿爾茨海默病的最強(qiáng)風(fēng)險(xiǎn)基因,APOE2則是保護(hù)基因,而APOE3則沒(méi)有特別的影響。但艾麗婭的病例顯示,基因之間存在相互作用,一種罕見(jiàn)突變可能對(duì)抗另一種。
艾麗婭的腦部影像顯示,β淀粉樣蛋白與tau蛋白似乎“斷絕關(guān)系”。
艾麗婭給世界留下了一個(gè)珍貴的禮物:她的大腦。借助單細(xì)胞 RNA 測(cè)序,研究人員得以揭示特定基因在腦細(xì)胞中的表達(dá)方式。最近的研究發(fā)現(xiàn),她的tau蛋白病理發(fā)展,在很大程度上“放過(guò)”了對(duì)判斷和其他執(zhí)行功能很重要的額葉皮質(zhì),以及對(duì)記憶和學(xué)習(xí)很重要的海馬體,轉(zhuǎn)而涉及了枕葉皮層,即控制視覺(jué)感知的頭部后部大腦區(qū)域。枕葉皮質(zhì)是唯一表現(xiàn)出典型阿爾茨海默癥特征的主要大腦區(qū)域,例如稱為小膠質(zhì)細(xì)胞的保護(hù)性腦細(xì)胞的慢性炎癥,和降低的APOE表達(dá)水平。【1】
還有一種罕見(jiàn)的APOE3變體APOE3-Jacksonville,也可以降低一個(gè)人患阿爾茨海默病的風(fēng)險(xiǎn)。自2014年被報(bào)道以來(lái),直到去年科學(xué)家才揭示它背后的潛在機(jī)制是減少APOE的自聚集,這與促進(jìn)膽固醇排出和增強(qiáng)的脂質(zhì)結(jié)合能力有關(guān),可以降低淀粉樣蛋白負(fù)荷和相關(guān)毒性,促進(jìn)大腦的修復(fù)和健康老化。【2】
“對(duì)阿爾茨海默病和認(rèn)知衰退有抵抗力的患者,正在引領(lǐng)我們對(duì)阿爾茨海默病病理生理學(xué)理解的一場(chǎng)革命,并為新的、受患者啟發(fā)的療法鋪平道路。”麻省總醫(yī)院多文化阿爾茨海默癥預(yù)防項(xiàng)目(MAPP)主任、哈佛醫(yī)學(xué)院精神病學(xué)副教授亞基爾·基羅斯(Yakeel T. Quiroz)參與領(lǐng)導(dǎo)了APOE3 Christchurch的研究。她認(rèn)為,APOE3-Jacksonville與硫酸乙酰肝素蛋白聚糖的相互作用受損,可能是與認(rèn)知癥風(fēng)險(xiǎn)降低相關(guān)的 APOE 變體(包括 APOE3-Christchurch 和 APOE2)的共同特征,需要進(jìn)一步研究。
進(jìn)入基因組“暗物質(zhì)”研究
早期發(fā)現(xiàn)的阿爾茨海默病基因,如導(dǎo)致早發(fā)性阿爾茨海默病的APP、PSEN1、PSEN2,和晚發(fā)性阿爾茨海默病的主要風(fēng)險(xiǎn)基因AOPE,都與加速淀粉樣蛋白沉積有關(guān)。2008年,阿爾茨海默病基因研究先驅(qū)魯?shù)婪颉ぬ过R(Rudolph Tanzi)的實(shí)驗(yàn)室,首次發(fā)現(xiàn)與神經(jīng)炎癥相關(guān)的阿爾茨海默基因CD33,它攜帶著小膠質(zhì)細(xì)胞上受體的遺傳密碼。
小膠質(zhì)細(xì)胞通常充當(dāng)大腦的管家之一,清除神經(jīng)碎片,包括斑塊和纏結(jié)。5年后,坦齊和他的同事們研究發(fā)現(xiàn),CD33影響小膠質(zhì)細(xì)胞的活動(dòng):當(dāng)該基因高度表達(dá)時(shí),小膠質(zhì)細(xì)胞會(huì)從管家轉(zhuǎn)變?yōu)樯窠?jīng)元?dú)⑹郑瑥亩l(fā)神經(jīng)炎癥。此后,與CD33具有相反作用的另一個(gè)阿爾茨海默基因TREM2也被發(fā)現(xiàn),它可以關(guān)閉小膠質(zhì)細(xì)胞促進(jìn)神經(jīng)炎癥的能力。
這或許能夠與部分特殊病例相印證:他們?cè)谑瑱z中被發(fā)現(xiàn)腦部有大量淀粉樣斑塊和神經(jīng)元纖維纏結(jié),卻始終沒(méi)有出現(xiàn)阿爾茨海默病癥狀,原因就在于他們沒(méi)有神經(jīng)炎癥。用坦齊的比喻來(lái)說(shuō),感染點(diǎn)燃了淀粉樣蛋白病變的火柴,隨著蛋白積累,殺死神經(jīng)元,引發(fā)神經(jīng)炎癥,隨后才蔓延為腦內(nèi)的“叢林大火”。
魯?shù)婪颉ぬ过R在線上演講中,介紹神經(jīng)炎癥在阿爾茨海默發(fā)病機(jī)制中的重要性。
今年4月,一項(xiàng)迄今為止最大規(guī)模、涉及10萬(wàn)患者和60萬(wàn)健康人的全基因組關(guān)聯(lián)研究結(jié)果出爐。在識(shí)別出的75個(gè)與阿爾茨海默有關(guān)的基因組區(qū)域中,新發(fā)現(xiàn)了42種阿爾茨海默基因,同樣將阿爾茨海默病與大腦免疫系統(tǒng)受損聯(lián)系了起來(lái)。【3】
“創(chuàng)建一個(gè)廣泛的阿爾茨海默病風(fēng)險(xiǎn)基因列表,就像一個(gè)大型拼圖過(guò)程,這項(xiàng)工作雖然沒(méi)有為我們提供完整的畫(huà)面,但給出了寶貴的框架。當(dāng)然,它也告訴我們阿爾茨海默癥有多么復(fù)雜,多種不同機(jī)制影響著疾病發(fā)展。”英國(guó)阿爾茨海默癥研究中心的研究主任蘇珊·科爾哈斯(Susan Kohlhaas)說(shuō)道。
不過(guò),僅僅有全基因組關(guān)聯(lián)研究(GWAS)或許仍然不夠。阿爾茨海默病的遺傳力(即遺傳變異占表現(xiàn)型總變異的百分?jǐn)?shù))估計(jì)在60%-80%之間。“APOE,APP,PSEN1和PSEN2,加上前40個(gè)GWAS基因,僅占阿爾茨海默病遺傳風(fēng)險(xiǎn)的一半,剩下的另一半未知,這是我們進(jìn)入基因組‘暗物質(zhì)’的地方——罕見(jiàn)變異。”坦齊曾說(shuō)到,罕見(jiàn)變異在人群中的發(fā)生頻率低于1%,卻占個(gè)體基因組變異的77%。【4】
去年4月,坦齊和同事們利用全基因組測(cè)序(WGS),發(fā)表了新發(fā)現(xiàn)的13 個(gè)與阿爾茨海默病有關(guān)的罕見(jiàn)變異基因。它們可以提供阿爾茨海默病與神經(jīng)發(fā)育、突觸功能(傳遞化學(xué)和電通訊信號(hào)的腦細(xì)胞之間的連接)和神經(jīng)可塑性(神經(jīng)元重組神經(jīng)元的能力)之間的一些最初的遺傳聯(lián)系。【5】“我們相信我們已經(jīng)創(chuàng)建了一個(gè)新模板,用于超越標(biāo)準(zhǔn) WGS以及疾病與常見(jiàn)基因組變異的關(guān)聯(lián),其中你錯(cuò)過(guò)了疾病的大部分遺傳景觀。”
麻煩的是,罕見(jiàn)突變可能只發(fā)生在一個(gè)人或一個(gè)家庭中。 “在阿爾茨海默病測(cè)序項(xiàng)目中進(jìn)行全基因組測(cè)序的2萬(wàn)人中,54% 的單核苷酸多態(tài)性僅在一個(gè)人身上看到,”斯坦福大學(xué)博士揚(yáng)·勒·根(Yann Le Guen)說(shuō)。如此小的樣本量要如何確定與阿爾茨海默病的關(guān)聯(lián)?功能多組學(xué)分析是關(guān)鍵策略。
罕見(jiàn)基因變異堪稱基因組中的“暗物質(zhì)”。
罕見(jiàn)基因變異能告訴我們什么
尋找阿爾茨海默罕見(jiàn)功能基因變異的研究通常分為三類:一是在已知關(guān)聯(lián)基因中尋找罕見(jiàn)功能變異,例如錯(cuò)義突變、插入/缺失、剪接變體、移碼和早期終止密碼子等;二是系統(tǒng)運(yùn)用全基因組測(cè)序 (WGS) 和基于全外顯子組測(cè)序 (WES) 數(shù)據(jù),來(lái)識(shí)別罕見(jiàn)的功能變異;三是在新的假設(shè)驅(qū)動(dòng)阿爾茨海默病的候選基因中,尋找罕見(jiàn)功能基因變異。一些罕見(jiàn)的基因變異簇還可以識(shí)別疾病相關(guān)的新基因,或表明已知疾病相關(guān)蛋白的哪個(gè)域可能出現(xiàn)故障。
今年4月,俄亥俄州克利夫蘭凱斯西儲(chǔ)大學(xué)的研究團(tuán)隊(duì),從大約5500個(gè)阿爾茨海默病例和 5000個(gè)阿爾茨海默測(cè)序項(xiàng)目(ADSP)對(duì)照的WES數(shù)據(jù)著手,在近21000個(gè)基因中識(shí)別出超過(guò)160萬(wàn)個(gè)罕見(jiàn)變異。再將這些變異映射到蛋白質(zhì)數(shù)據(jù)庫(kù)中的6000多種蛋白質(zhì)結(jié)構(gòu),以及人工智能 AlphaFold 推定的近 17500 個(gè)蛋白質(zhì)結(jié)構(gòu)上,發(fā)現(xiàn)只有少數(shù)相應(yīng)基因具有統(tǒng)計(jì)顯著性的罕見(jiàn)基因變異簇。
隨后再在一個(gè)ADSP WES獨(dú)立隊(duì)列中搜索這些基因變異熱點(diǎn),最后鎖定了三個(gè)基因:除了已知的TREM2和 SORL1,還有一個(gè)全新的基因EXOC3L4。它表達(dá)一種過(guò)去知之甚少的蛋白質(zhì),預(yù)計(jì)是外囊復(fù)合物的一個(gè)組成部分,參與囊泡運(yùn)輸和胞吐作用。
在這項(xiàng)研究的分析中,這三個(gè)基因的突變數(shù)分別達(dá)到33、56和68個(gè)。在阿爾茨海默病例中,有15個(gè)EXOC3L4變體落入 C 端 Sec6 域。【6】此前研究顯示,該領(lǐng)域內(nèi)的罕見(jiàn)變異與阿爾茨海默病的皮質(zhì)葡萄糖代謝有關(guān)。
“這項(xiàng)研究提出的評(píng)估罕見(jiàn)錯(cuò)義變異同時(shí)考慮其在蛋白質(zhì)中的空間分布的統(tǒng)計(jì)方法,在阿爾茨海默病研究領(lǐng)域是新穎的,特別有助于聚合在空間上聚集在一起的單例。”揚(yáng)·勒·根評(píng)價(jià),這為未來(lái)的藥物開(kāi)發(fā)提供了信息,即應(yīng)該針對(duì)蛋白質(zhì)的哪個(gè)結(jié)構(gòu)域會(huì)對(duì)疾病產(chǎn)生影響。
“目前大約有100種阿爾茨海默相關(guān)的基因變異已經(jīng)被確認(rèn),其中大約一半是保護(hù)性的,一半是危險(xiǎn)因素,其中大多數(shù)還沒(méi)有被確認(rèn)的功能。”坦齊認(rèn)為,接下來(lái)的問(wèn)題是如何評(píng)估個(gè)體的風(fēng)險(xiǎn),許多團(tuán)隊(duì)正在開(kāi)發(fā)多基因風(fēng)險(xiǎn)評(píng)分,“一個(gè)好的多基因風(fēng)險(xiǎn)評(píng)分,不依賴于單個(gè)基因和基因功能,而是基于基因組單個(gè)片段的遺傳模式。”
“識(shí)別已確立和新的候選阿爾茨海默基因中的罕見(jiàn)功能變異,有望加速阿爾茨海默病遺傳數(shù)據(jù)轉(zhuǎn)化為有意義的生物學(xué)數(shù)據(jù),并更好地理解阿爾茨海默病,以及如何治療這種毀滅性的疾病。”坦齊說(shuō)。
-
世界聚焦:投資3億元,輕舟智航擬在安陽(yáng)設(shè)立無(wú)人巴士產(chǎn)線
頭條 22-09-22
-
【環(huán)球速看料】剛剛!河南創(chuàng)新投資集團(tuán)揭牌
頭條 22-09-22
-
焦點(diǎn)資訊:河南昨日新增本土無(wú)癥狀感染者6例
頭條 22-09-22
-
天天熱推薦:隔夜歐美·9月22日
頭條 22-09-22
-
每日看點(diǎn)! 立方風(fēng)控鳥(niǎo)·早報(bào)(9月22日)
頭條 22-09-22
-
今日快訊:皮海洲:上市公司回購(gòu)如潮 為何難以提振股價(jià)?
頭條 22-09-22
-
焦點(diǎn)熱文:同心傳動(dòng)簽訂1.13億元年度框架合同
頭條 22-09-21
-
環(huán)球最資訊丨鄭州收購(gòu)首批2萬(wàn)套(間)存量房源用于人才公寓
頭條 22-09-21
-
全球熱頭條丨立方風(fēng)控鳥(niǎo)·晚報(bào)(9月21日)
頭條 22-09-21
-
快播:全省首家!河南省科學(xué)院鶴壁分院揭牌成立
頭條 22-09-21
-
速訊:地標(biāo)農(nóng)產(chǎn)品上行加速,河南鐵棍懷山藥、稻田活蝦等最受歡迎
頭條 22-09-21
-
環(huán)球焦點(diǎn)!券商研究所大調(diào)研!中證協(xié)發(fā)文
頭條 22-09-21
-
全球速讀:光力科技二股東減持318.3萬(wàn)股,持股降至5%以下
頭條 22-09-21
-
全球短訊!今起,商丘將在11家超市投放政府儲(chǔ)備豬肉,價(jià)格公布
頭條 22-09-21
-
焦點(diǎn)信息:總投資159.98億元,河南2條高速公路項(xiàng)目主體施工圖獲批
頭條 22-09-21
-
快看點(diǎn)丨河南天馬新材完成發(fā)行1656.7萬(wàn)股新股,募資3.54億元
頭條 22-09-21
-
快播:河南首臺(tái)智慧儲(chǔ)能液冷柜式產(chǎn)品下線
頭條 22-09-21
-
世界速看:河南昨日新增本土無(wú)癥狀感染者8例
頭條 22-09-21
-
【天天時(shí)快訊】養(yǎng)老金,又有新變化
頭條 22-09-21
-
環(huán)球速遞!隔夜歐美·9月21日
頭條 22-09-21
-
環(huán)球觀速訊丨立方風(fēng)控鳥(niǎo)·晚報(bào)(9月20日)
頭條 22-09-20
-
環(huán)球頭條:鄭州保交樓出臺(tái)新舉措:交房即發(fā)證
頭條 22-09-20
-
全球視訊!平煤股份獲批注冊(cè)20億元PPN
頭條 22-09-20
- 【環(huán)球速看料】困在時(shí)間里|尋找阿爾茨海默2022-09-22
- 深耕全域旅游賽道,萍鄉(xiāng)武功山打出一套“組2022-09-22
- 美樂(lè)童年DIY丙烯筆,守護(hù)孩子童真童趣2022-09-22
- u盤(pán)驅(qū)動(dòng)程序怎么安裝?U盤(pán)萬(wàn)能驅(qū)動(dòng)如何進(jìn)行2022-09-22
- 頗具“顛覆者”實(shí)力,艾瑞澤8雖未上市,但2022-09-22
- 電腦死機(jī)按什么鍵恢復(fù)?電腦經(jīng)常死機(jī)怎么辦2022-09-22
- 臺(tái)式電腦怎么看電腦配置高低?買(mǎi)電腦主要看2022-09-22
- 電腦插入移動(dòng)硬盤(pán)參數(shù)錯(cuò)誤打不開(kāi)怎么辦?移2022-09-22
- 固態(tài)硬盤(pán)4k對(duì)齊什么意思?固態(tài)硬盤(pán)分區(qū)為什2022-09-22
- 電腦系統(tǒng)注冊(cè)表?yè)p壞怎么修復(fù)?PE修復(fù)系統(tǒng)步2022-09-22
- 電腦系統(tǒng)權(quán)限受限如何解除?電腦連接wifi顯2022-09-22
- 筆記本電腦磁盤(pán)分區(qū)后怎么合并?電腦有幾種2022-09-22
- u盤(pán)寫(xiě)保護(hù)怎么解除?u盤(pán)有寫(xiě)保護(hù)怎么強(qiáng)制格2022-09-22
- Outlook怎么安裝?outlook在哪里打開(kāi)?2022-09-22
- 貨幣基金爆倉(cāng)是什么意思?貨幣基金看萬(wàn)份收2022-09-22
- 人民幣匯率破7的利弊有哪些?人民幣匯率破72022-09-22
- 工商銀行類似余額寶的叫什么?余額寶利率和2022-09-22
- 短期小額理財(cái)有哪些方式?小額資金怎么理財(cái)2022-09-22
- 余額寶什么時(shí)候推出的?余額寶幾點(diǎn)計(jì)算收益2022-09-22
- 中信銀行信用卡的積分怎么使用?中信銀行積2022-09-22
- 汽車(chē)保險(xiǎn)第二年比第一年便宜多少?車(chē)險(xiǎn)不出2022-09-22
- 網(wǎng)上銀行跨行轉(zhuǎn)賬要手續(xù)費(fèi)嗎?網(wǎng)上銀行跨行2022-09-22
- 科創(chuàng)50ETF是什么?科創(chuàng)50和科創(chuàng)50ETF的區(qū)別2022-09-22
- 建行龍卡信用卡額度是多少? 建行龍卡信用2022-09-22
- 什么是IPO?上市公司要多少資產(chǎn)可以上市?2022-09-22
- 欣旺達(dá)加碼動(dòng)力電池 目標(biāo)要做到國(guó)內(nèi)前三2022-09-22
- 馬可波羅沖擊IPO 壞賬風(fēng)險(xiǎn)等備受關(guān)注2022-09-22
- 半年報(bào)顯示:知名基金經(jīng)理上半年賠了76億元2022-09-22
- 招行首批落地 外幣ESG債券回購(gòu)業(yè)務(wù)2022-09-22
- 近期市場(chǎng)的持續(xù)調(diào)整和股價(jià)的回落 多家公司2022-09-22
精彩推薦
閱讀排行
- 《河南省大數(shù)據(jù)產(chǎn)業(yè)發(fā)展行動(dòng)計(jì)劃(2022-2025)》出臺(tái) 建全國(guó)領(lǐng)先大數(shù)據(jù)產(chǎn)業(yè)創(chuàng)新發(fā)展區(qū)
- 河南省干熱巖資源研究成果達(dá)到國(guó)內(nèi)領(lǐng)先水平
- 河南銀保監(jiān)局發(fā)布提示: 警惕非法“代理退保”陷阱 做到理性消費(fèi)和依法維權(quán)
- 本年度河南最大規(guī)模“招聘會(huì)”即將上線!參會(huì)單位3239家
- 河南2條高速公路項(xiàng)目主體施工圖獲批 總投資159.98億元
- 河南8月環(huán)境空氣質(zhì)量排名出爐 平頂山躍居第一駐馬店墊底
- 2022年國(guó)家綜合貨運(yùn)樞紐補(bǔ)鏈強(qiáng)鏈?zhǔn)着鞘泄?鄭州入選
- 冷空氣又來(lái)啦!河南22日短暫升溫 23日降溫+大風(fēng)來(lái)襲
- 前沿資訊!今評(píng)彈|任職要求寫(xiě)11遍“膚白貌美大長(zhǎng)腿”,招聘豈能無(wú)底線的“皮”
- 全球看點(diǎn):【視頻】設(shè)計(jì)河南建設(shè)工作會(huì)議召開(kāi)
要聞
《河南省大數(shù)據(jù)產(chǎn)業(yè)發(fā)展行動(dòng)計(jì)劃(2
河南省干熱巖資源研究成果達(dá)到國(guó)內(nèi)
河南銀保監(jiān)局發(fā)布提示: 警惕非法
- 《河南省大數(shù)據(jù)產(chǎn)業(yè)發(fā)展行動(dòng)計(jì)劃(2
- 河南省干熱巖資源研究成果達(dá)到國(guó)內(nèi)
- 河南銀保監(jiān)局發(fā)布提示: 警惕非法
- 本年度河南最大規(guī)模“招聘會(huì)”即將
- 河南2條高速公路項(xiàng)目主體施工圖獲批
- 河南8月環(huán)境空氣質(zhì)量排名出爐 平頂
- 2022年國(guó)家綜合貨運(yùn)樞紐補(bǔ)鏈強(qiáng)鏈?zhǔn)?/a>
- 冷空氣又來(lái)啦!河南22日短暫升溫 2
- 前沿資訊!今評(píng)彈|任職要求寫(xiě)11遍“
- 全球看點(diǎn):【視頻】設(shè)計(jì)河南建設(shè)工